1.2. CẤU TẠO CỦA KIM LOẠI VÀ HỢP KIM
1.2.1. Cấu tạo của kim loại
a. Khái niệm về kim loại
Định nghĩa
Kim loại là vật thể sáng, dẻo có thể rèn được, có tính dẫn nhiệt và dẫn điện cao.
Cấu tạo mạng tinh thể của kim loại
- Trong điều kiện thường và áp suất khí quyển hầu hết các kim loại tồn tại ở trạng thái rắn (ngoại trừ thủy ngân).
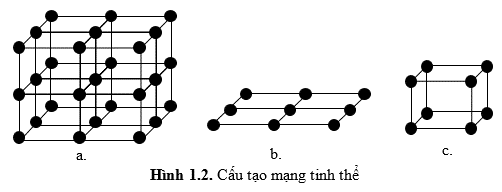
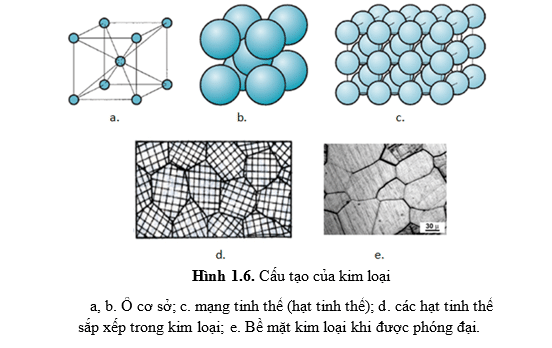
- Mạng tinh thể là mô hình hình học mô tả sự sắp xếp có quy luật của các nguyên tử (phân tử) trong không gian (Hình 1.2 a).
- Mạng tinh thể bao gồm các mặt đi qua các nguyên tử, các mặt này luôn luôn song song cách đều nhau và được gọi là mặt tinh thể (Hình 1.2 b).
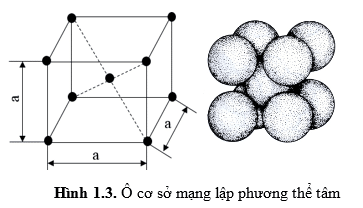
- Ô cơ sở là hình khối nhỏ nhất có cách sắp xếp chất điểm đại diện chung cho mạng tinh thể (Hình 1.2 c). Trong thực tế để đơn giản chỉ cần biểu diễn mạng tinh thể bằng ô cơ sở của nó là đủ. Tuỳ theo loại ô cơ bản người ta xác định các thông số mạng. Ví dụ như trên ô lập phương thể tâm (Hình 1.3) có thông số mạng là a là chiều dài cạnh của ô. Đơn vị đo của thông số mạng là Ăngstrong (Angstrom), ký hiệu: A
Các kiểu mạng tinh thể thường gặp:
- Mạng lập phương thể tâm: các nguyên tử (ion) nằm ở các đỉnh và ở tâm của khối lập phương.
Các kim loại nguyên chất có kiểu mạng này như: Feα , Cr, W, Mo, V…
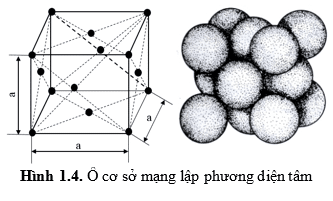
- Lập phương diện tâm: các nguyên tử (ion) nằm ở các đỉnh và giữa (tâm) các mặt của hình lập phương.
Các kim loại nguyên chất có kiểu mạng này như: Feg, Cu, Ni, Al, Pb…
- Lục giác xếp chặt: bao gồm 12 nguyên tử nằm ở các đỉnh, 2 nguyên tử nằm ở giữa 2 mặt đáy của hình lăng trụ lục giác và 3 nguyên tử nằm ở khối tâm của 3 lăng trụ tam giác cách đều nhau
Các kim loại nguyên chất có kiểu mạng này như: Mg, Zn…
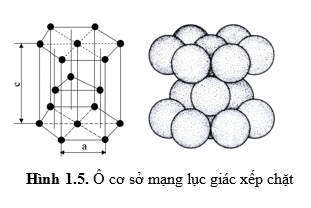
Như vậy có thể xem một khối kim loại nguyên chất là tập hợp vô số các mạng tinh thể (hạt tinh thể) được sắp xếp hỗn độn, mạng tinh thể lại gồm vô số các ô cơ sở và dạng của từng ô cơ sở tùy thuộc vào kiểu mạng của kim loại đó.
b. Tính thù hình của kim loại
Định nghĩa
Là một kim loại có thể có nhiều kiểu mạng tinh thể khác nhau tồn tại ở những khoảng nhiệt độ và áp suất khác nhau.
Đặc tính thù hình
- Các dạng thù hình khác nhau được ký hiệu bằng các chữ cái Hy Lạp theo nhiệt độ từ thấp đến cao: α, β, γ, δ…
- Khi có chuyển biến thù hình thì kim loại có sự thay đổi thể tích và tính chất bên trong. Đây là đặc tính quan trọng khi sử dụng chúng.
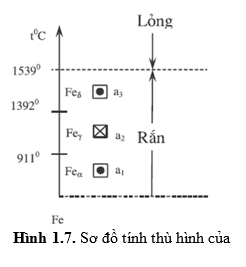
Ví dụ: Khi nung nóng sắt người ta thấy ở trạng thái rắn sắt thay đổi ba kiểu mạng tinh thể ở ba khoảng nhiệt độ khác nhau (≤ 9110C, 911 – 13920C, ≥ 13920C). Vậy sắt có ba dạng thù hình được ký hiệu là: Feα, Feg, Feδ. Ta thấy sắt có ba kiểu mạng tinh thể khác nhau do đó tính chất của sắt ứng với từng kiểu mạng cũng khác nhau.
1.2.2. Cấu tạo của hợp kim
a. Khái niệm về hợp kim
Định nghĩa
Hợp kim là vật thể có chứa nhiều nguyên tố và mang tính chất kim loại. Nguyên tố chủ yếu trong hợp kim là nguyên tố kim loại.
Ưu điểm của hợp kim so với kim loại
Trong lĩnh vực cơ khí, hợp kim được sử dụng rộng rãi vì các ưu điểm sau:
- Cơ tính hợp kim phù hợp với vật liệu chế tạo cơ khí: đối với ngành cơ khí vật liệu sử dụng phải có các yêu cầu như độ bền cao, tuổi thọ sử dụng lâu. Về mặt này thì hợp kim hơn hẳn kim loại nguyên chất, chúng có độ cứng, độ bền cao hơn hẳn trong khi độ dẻo và độ dai vẫn đủ cao.
- Tính công nghệ thích hợp: kim loại nguyên chất có tính dẻo cao dễ gia công áp lực nhưng khó đúc, gia công cắt kém, không hóa bền được bằng nhiệt luyện. Hợp kim có tính công nghệ khác nhau và phù hợp với từng điều kiện gia công: gia công áp lực ở trạng thái nóng và nguội, đúc, gia công cắt, nhiệt luyện… đảm bảo cho chế tạo sản phẩm có năng suất cao.
- Giá thành hạ hơn: dễ chế tạo hơn do không phải khử bỏ các tạp chất một cách triệt để như kim loại.
b. Các dạng cấu tạo của hợp kim
Có thể nói tính chất của hợp kim phụ thuộc vào sự kết hợp của các nguyên tố cấu tạo nên chúng. Khi ở dạng lỏng, các nguyên tố hòa tan lẫn nhau để tạo nên dung dịch lỏng. Tuy nhiên, khi làm nguội ở trạng thái rắn sẽ hình thành các tổ chức pha của hợp kim, có thể sẽ rất khác nhau do tác dụng với nhau giữa các nguyên tố. Có thể có các tổ chức pha như sau:
Tổ chức một pha (một kiểu mạng tinh thể):
- Khi các nguyên tố trong hợp kim tác dụng hòa tan ở trạng thái rắn, gọi là dung dịch rắn.
- Khi các nguyên tố trong hợp kim tác dụng hóa học ở trạng thái rắn, gọi là hợp chất hóa học.
- Tổ chức hai pha trở lên (có từ hai kiểu mạng tinh thể trở lên): khi giữa các pha trong hợp kim có tác dụng cơ học với nhau gọi là hỗn hợp cơ học.
Dung dịch rắn
Khi nguyên tử của hai hay nhiều nguyên tố được sắp xếp trong cùng một kiểu mạng. Có thể chia dung dịch rắn làm hai loại: dung dịch rắn xen kẽ và dung dịch rắn thay thế.
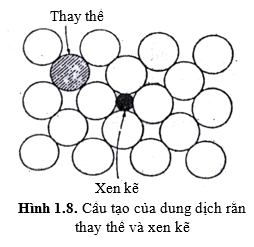
- Dung dịch rắn xen kẽ. Nếu nguyên tử của nguyên tố hòa tan (B) xen kẽ ở khoảng hở của các nguyên tử trong dung môi (A) thì ta có dung dịch rắn xen kẽ. Sự hòa tan xen kẽ bao giờ cũng có giới hạn.
- Dung dịch rắn thay thế. Nếu nguyên tử của nguyên tố hòa tan (B) thay thế nguyên tử của nguyên tố dung môi (A) thì ta có dung dịch rắn thay thế.
Cơ tính chung của dung dịch rắn: có độ cứng thấp, độ bền thấp tuy nhiên độ dẻo và độ dai cao do có cấu tạo mạng tinh thể của kim loại nguyên chất.
Hợp chất hóa học
Trong nhiều loại hợp kim, nhiều pha được tạo thành do sự liên kết giữa các nguyên tố khác nhau theo một tỷ lệ nhất định gọi là hợp chất hóa học. Mạng tinh thể của hợp chất khác với mạng thành phần. Hợp chất hóa học trong hệ có tính ổn định cao hoặc có nhiều dạng hợp chất khác nhau.
Ví dụ: Nguyên tố sắt và cacbon tạo nên Fe3C rất ổn định, nhưng nguyên tố Cu với Zn có thể cho ta nhiều dạng hợp chất như: CuZn, Cu3Zn3, CuZn3,…
Cơ tính chung của hợp chất hóa học: có độ cứng cao, độ dòn cao do có kiểu mạng tinh thể phức tạp không giống với kiểu mạng của kim loại nguyên chất đồng thời có nhiệt độ phân hủy cao (t0nc cao).
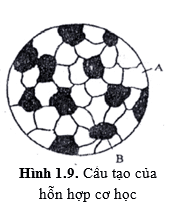
Hỗn hợp cơ học
Trong hệ hợp kim, có những nguyên tố không hòa tan vào nhau cũng không liên kết tạo thành hợp chất hóa học mà chỉ liên kết với nhau bằng lực cơ học thuần túy, thì gọi hợp kim đó là hỗn hợp cơ học. Như vậy hỗn hợp cơ học không làm thay đổi mạng nguyên tử của nguyên tố thành phần. Vì để tạo được liên kết cơ học nguyên tử các nguyên tố thành phần khác nhau nhiều về kích thước và mạng tinh thể.
Cơ tính chung của hỗn hợp cơ học: phụ thuộc vào cơ tính của các pha tạo thành. Muốn đánh giá cơ tính của hợp kim tạo thành tại nhiệt độ xác định phải căn cứ vào tỉ lệ cấu tạo và cơ tính của các pha tạo thành.